| سرطان الخلايا العملاقة في الرئة | |
|---|---|
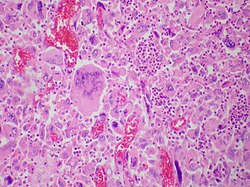 سرطان الخلايا الرئوية العملاقة يُمثل نوعًا نادرًا من سرطانات الرئة غير صغيرة الخلايا، يتميز بوجود العديد من خلايا الورم العملاقة وتدفق الخلايا الالتهابية، وهي في الغالب كريات بيضاء متعددة النوى ممزوجة بالبلعميات. من المحتمل أن تكون التجمعات البيضاوية الكثيفة من كريات الدم البيضاء متعددة النوى، الظاهرة في هذه الصورة، موجودة في سيتوبلازم خلايا الورم العملاقة (التكوّن الإمبريالي) التي قُطعت في مستوى لا يشمل نواتها.
| |
| معلومات عامة | |
| الاختصاص | علم الأورام |
| من أنواع | سرطانة الخلايا الكبيرة في الرئة ، وسرطان الرئة الساركوماتوئيدي |
| تعديل مصدري - تعديل | |
سرطان الخلايا العملاقة في الرئة (اختصارًا GCCL) هو شكل نسيجي نادر من سرطان الخلايا الكبيرة في الرئة، وهو نوع فرعي من سرطان الرئة غير المتمايز، يصنف تقليديًا ضمن سرطانات الرئة غير صغيرة الخلايا (NSCLC). السمة المميزة لهذا الورم الخبيث المميت للغاية هي المظهر المجهري الضوئي المميز لخلاياه الكبيرة للغاية، وهي غريبة ومتعددة الأشكال للغاية، والتي غالبًا تحتوي على أكثر من نواة ضخمة مشوهة ومتعددة الأشكال ("syncytia")، والتي تنتج عن اندماج الخلايا. على الرغم من أنه من الشائع في أدبيات سرطان الرئة الإشارة إلى الأورام المختلطة نسيجيًا التي تحتوي على أعداد كبيرة من الخلايا العملاقة الخبيثة باسم "سرطانات الخلايا العملاقة"، إلا أنه من الناحية الفنية يجب أن يقتصر تشخيص "سرطان الخلايا العملاقة" بشكل صارم على الأورام التي تحتوي فقط على خلايا عملاقة خبيثة (أي سرطان الخلايا العملاقة "النقي").[1] بصرف النظر عن التباين الكبير الذي يُرى في سرطانات الرئة (خاصة تلك التي تحدث بين مدخني التبغ)، فإن التباين الكبير في تقنيات التشخيص وأخذ العينات المستخدمة في الممارسة الطبية، والنسبة المتباينة العالية للأفراد الذين يُشتبه في إصابتهم بسرطان الخلايا العملاقة والذين لا يخضعون لاستئصال جراحي كامل، والافتقار شبه العالمي للتقطيع الكامل والفحص المرضي لعينات الورم المستأصلة تمنع المستويات الكمية عالية الدقة.
التصنيف
لعقود عديدة، صُنفت سرطانات الرئة الأولية بشكل ثنائي لأغراض العلاج والبحث إلى سرطانات رئوية صغيرة الخلايا (SCLCs) وسرطانات رئوية غير صغيرة الخلايا (NSCLCs)، بناءً على نهج مُبسط للغاية أصبح عفا عليه الزمن الآن. يُقرّ النموذج الجديد بأن سرطانات الرئة تُشكّل عائلة كبيرة ومتباينة للغاية من الأورام الخبيثة،[2] مع أكثر من 50 نوعًا نسيجيًا مختلفًا مُدرجًا في المراجعة الرابعة (2004) لنظام تصنيف منظمة الصحة العالمية، وهو نظام تصنيف سرطان الرئة الأكثر استخدامًا ("WHO-2004").[1] تقدّر هذه المتغيرات بشكل متزايد على أنها ذات خصائص وراثية وبيولوجية وسريرية مختلفة، وكذلك التشخيص والاستجابة لأنظمة العلاج، لذلك، فإن التصنيف النسيجي الصحيح والمتسق لسرطانات الرئة ضروري للتحقق من صحة استراتيجيات الإدارة المثلى وتنفيذها.[3][4] حوالي 1% من سرطانات الرئة هي ساركوما وأورام الخلايا الجرثومية وأورام مكونة للدم، بينما 99% من سرطانات الرئة هي سرطانة. السرطانات هي أورام تتكون من خلايا غير طبيعية متحولة ذات بنية نسيجية ظهارية و/أو خصائص جزيئية، والتي تنشأ من الأديم الباطن الجنيني.[5] قد حدد ثمانية أنواع رئيسية من سرطانات الرئة ضمن تصنيف منظمة الصحة العالمية لعام 2004:[1]
- سرطان الخلايا الصغيرة
- سرطان الخلايا الحرشفية
- سرطان الغدد
- سرطان الخلايا الكبيرة
- سرطان الغدد الحرشفية
- سرطان الساركوماتويد
- سرطان السرطاوي
- سرطان الغدد اللعابية
شهد التصنيف الفرعي لسرطان الخلايا العملاقة للرئة بين هذه الأنواع الرئيسية تغييرات كبيرة في العقود الأخيرة. وفي المراجعة الثانية (1981) لتصنيف منظمة الصحة العالمية، اعتُبر نوعًا فرعيًا من سرطان الخلايا الكبيرة.[6] في المراجعة الثالثة (1999)،[7] وُضعت ضمن تصنيف يسمى "السرطانات ذات العناصر متعددة الأشكال أو الساركوماتويدية أو الساركومية"، إلى جانب السرطان متعدد الأشكال وسرطان الخلايا المغزلية والساركوما السرطانية وورم الأرومة الرئوية، والتي (يمكن القول) أنها متغيرات مترابطة. حُفظت المراجعة الرابعة بنفس مجموعة المشاكل مثل المراجعة الثالثة، تم اختصار اسم التصنيف الرئيسي إلى "سرطانات الساركوماتويدية".[1] القواعد الحالية لتصنيف سرطانات الرئة بموجب منظمة الصحة العالمية، وعلى الرغم من فائدتها وتحسينها، تظل إلى حد ما معقدة إلى حد ما وغامضة وتعسفية وغير كاملة.[1] على الرغم من شيوع تسمية الأورام المختلطة التي تحتوي على خلايا عملاقة خبيثة بـ"سرطانات الخلايا العملاقة"، إلا أن التصنيف الدقيق لورم رئوي كسرطان خلايا عملاقة خبيثة يتطلب أن يتكون الورم بأكمله من خلايا عملاقة خبيثة فقط. لذلك، يُعدّ أخذ عينة كاملة من الورم بأكمله - عن طريق الاستئصال الجراحي - ضروريًا للغاية لتشخيص سرطان الخلايا العملاقة الخبيثة بشكل قاطع.[1]
علم الخلايا
احتوت الخلفية على العديد من الخلايا الليمفاوية والخلايا المتعادلة. كان شكل خلية الورم مغزليًا أو متعدد الأشكال، وتفاوتت أحجام خلايا الورم بأكثر من خمسة أضعاف. احتوت خلايا الورم على سيتوبلازم كثير وسميك ومحدد المعالم. كان موقع النواة طرديًا مركزيًا، وكانت النواة بيضاوية أو غير منتظمة الشكل. لوحظت خلايا عملاقة متعددة النوى بشكل متكرر. كان حجم النواة أكبر بخمسة أضعاف من حجم الخلايا الليمفاوية الطبيعية، كما تفاوت حجمها بأكثر من خمسة أضعاف. كان الغشاء النووي رقيقًا، وكان الكروماتين النووي حبيبيًا بشكل خشن، بينما كانت النوية مفردة ومستديرة.في الاستعدادات الخلوية، تظهر الخلايا العملاقة عادةً كخلايا مفردة أو في مجموعات مسطحة فضفاضة، وأحيانًا في حزم.[8] يُعتبر سرطان الخلايا العملاقة للرئة أحد أكثر أنواع سرطان الرئة شيوعًا، ويُسمى "سرطان الخلايا غير الصغيرة". تشكل هذه المجموعة من الأورام القاتلة ما يقرب من 85% من جميع سرطانات الرئة.[1] وفقًا لتعريف "سرطان الخلايا الكبيرة مقابل الصغيرة"، يجب أن يكون قطر خلايا العملاقة أكبر بكثير من ثلاثة أضعاف قطر الخلايا الليمفاوية الساكنة (أي غير المحفزة). أيضًا وفقًا للتعريف، لا تحتوي الخلايا العملاقة على أي كمية من هذه الخلايا الصماء العصبية الصغيرة التي تحتوي على حبيبات إفرازية عصبية والتي تميز سرطانات الخلايا الصغيرة - عندما تحتوي عليها، يجب تصنيف الورم على أنه سرطان خلايا صغيرة مركب.[1] بالمقارنة مع معظم متغيرات سرطان الرئة الأخرى، تميل الخلايا المكونة الورم الخلايا العملاق إلى أن تكون أكبر بكثير (يصل قطرها إلى 150 ميكرومترًا، أو حتى أكبر)،[9] تُظهر كل من الخلايا والنوى تباينًا شديدًا في توزيع الحجم والشكل. أُبلغ أن متوسط حجم نوى سرطان الخلايا العملاقة السرطانية يبلغ 5 أضعاف حجم نوى الخلايا الليمفاوية.[8] تكون الخلايا من سرطانات الخلايا العملاقة غير متمايزة، ولا تظهر أي دليل على نضج الخلايا أو تمايزها، وتفتقر إلى الخصائص الخلوية والنسيجية لسرطان الخلايا الحرشفية، أو السرطان الغدي، أو سرطان الغدد الصم العصبية، أو أنواع خلايا سرطان الرئة الأخرى الأكثر تمايزًا. تميل إلى أن تكون متعددة الأشكال للغاية (أي متغيرة في الخصائص)، ولكنها غالبًا ما تكون مستديرة و/أو متعددة الأضلاع في الشكل، مع نسبة منخفضة نسبيًا من النواة إلى السيتوبلازم. عندما ترتبط بالخلايا المغزلية، كما هو الحال في كثير من الأحيان في الأورام ذات الأنسجة المختلطة، تميل الخلايا العملاقة الخبيثة إلى تكوين هياكل مجمعة متماسكة بشكل فضفاض عند الفحص الخلوي. مع ذلك، عندما تتكون عينة الخزعة من خلايا عملاقة خبيثة بحتة، تميل الخلايا إلى أن تكون مفردة ومتفككة.[1] تشير سلسلة الحالات إلى أن العدد النسبي للخلايا العملاقة في ورم معين يتناسب بشكل عام بشكل مباشر مع حجم الورم، ومع الكمية النسبية للنخر.[10] ترتبط الخلايا العملاقة في سرطان الرئة ارتباطًا وثيقًا بوجود الخلايا المغزلية.[11] يميل الكروماتين في الخلايا العملاقة الخبيثة إلى أن يكون مفرط اللون ومتكتلًا بشكل خشن. عادةً ما تكون النوى متعددة وبارزة.[9] تشمل الخصائص دون الخلوية التي غالبًا ما يتم ملاحظتها في الخلايا العملاقة الخبيثة لحالات ورم الخلايا العملاق الميتوكوندريا الوفيرة، ودوامات متحدة المركز من ألياف تشبه الخيوط التوترية، وتجمعات عدة أزواج من الجسيمات المركزية.[12] كل من "خلية ورم الخلايا السرطانية" و "خلية الكريات البيض - خلية الورم" (أي الاختراق النشط للأخير من قبل السابق) شائعة جدًا في حالات.[12]
السمات الهيكلية للأنسجة
في الأورام المختلطة، من المرجح أن توجد الخلايا العملاقة بنسب أعلى على حافة الورم.[11] عند وجود نخر واسع النطاق، من الممكن أن يحتوي ورم الخلايا العملاقة على حافة رقيقة فقط من الخلايا القابلة للحياة متبقية على محيط الكتلة. في أحد تسلسل الحالات المبكرة، لوحظ أن الإنتاج الوفير من الخلايا العملاقة الخبيثة يملأ الحويصلات الهوائية لدى المرضى دون تدمير أو تسلل أو إزعاج البنية الأساسية الطبيعية، وهو سلوك مرضي يشبه إلى حد ما المتغير الرئوي للسرطانة الغدية الرئوية. يُعد نخر الورم واسع النطاق والنزيف شائعًا للغاية في ورم الخلايا العملاقة. على الرغم من أن المشكلة لم تُدرس على نطاق واسع بطريقة خاضعة للرقابة، فقد لوحظ أن ورم الخلايا العملاقة تحتوي على مستويات مرتفعة بشكل كبير من عامل النمو الباطني الوعائي (VEGF).[13] مع ذلك، في إحدى الدراسات التي استُأصل فيها ورم سرطاني ذو خلايا عملاقة بالكامل، وخضع للفحص، لم تُلاحظ أي تشوهات نوعية أو كمية في تكوين الأوعية الدموية في الأنسجة.[9] لُوحظ أن خلايا ورم الخلايا العملاقة مُغلَّفة، ومُقسَّمة عبر الحواجز إلى "فصيصات زائفة"، بواسطة سدى ليفي، يُقترح أنه يُنتَج بالتناسب مع نمو الورم. عادةً ما تكون الكبسولة مملوءة بخلايا عملاقة خبيثة.[14]
السمات العيانية
تُظهر سرطانات الخلايا العملاقة في الرئة غالبًا نخرًا واسع النطاق وانحلال للغشاء المخاطي.[11][14] لُوحظ الاتجاه نحو قلة الأوعية الدموية وكثافة الأنسجة (مع انخفاض تعزيز التباين في التصوير المقطعي ) باتجاه مركز هذه الآفات، وخاصة في الأورام الأكبر حجمًا، وحتى في الأورام التي لا تحتوي على حجم كبير من النخر الكلي.[15] غالبًا ما تكون الأسطح المقطوعة لهذه الأورام الخبيثة رمادية-بيضاء أو سمراء، وغالبًا ما تُظهر بؤرًا مخاطية ونخرية.[15] غالبًا ما تُظهر هذه الأنواع من المناطق مستويات منخفضة من تعزيز التباين في التصوير المقطعي. يميل إلى ملاحظة انخفاض التغليف وارتفاع مستويات الكولاجين النسيجي، مع تعزيز تباين عالٍ في هذه المناطق.[15] وقد لوحظ تطور سرطان الخلايا العملاقة داخل فقاعات انتفاخية.[16]
التلوّن والكيمياء المناعية
أظهرت حالة نقائل دماغية من سرطان الرئة الخلايا العملاقة (كلاهما "نقي") نتائج إيجابية لسيتوكيراتينات AE1/AE3، وسلبية لـ CK-7 وCK-20 وTTF-1 وGFAP.[17] غالبًا ما تتلوّن خلايا ورم الخلايا العملاقة بشدة باستخدام كاشف حمض الدوري-شيف، مما يشير إلى وجود كميات كبيرة من الجليكوجين في سيتوبلازم الخلية. [14]
التشخيص التفريقي
تحت المجهر الضوئي، تشبه الخلايا الخبيثة متعددة الأشكال العملاقة التي تُشكّل ورم الخلايا العملاقة تلك الموجودة في سرطان المشيمة،[1] والساركوما الوعائية،[18] وبعض أشكال الساركوما الحقيقية،[1] مثل الورم النسيجي الليفي الخبيث،[1] والساركوما العضلية المخططة.[9] في بعض الحالات، يمكن أن تحمل أيضًا تشابهًا كبيرًا مع الخلايا النسيجية "المنشطة" التي تُرى في بعض الحالات الالتهابية.[9] تحدث معضلة تشخيصية تفاضلية نادرة وصعبة محتملة عندما يجب فصل ورم الخلايا العملاقة عن سرطانات المشيمية الرئوية أو المنصفية، وهو تمييز بالغ الأهمية يجب إجراؤه لأنه في حين يوجد معيار معروف للرعاية لعلاج سرطان المشيمة، إلا أنه لا يوجد حتى الآن علاج قياسي محدد مقبول بشكل عام لـورم الخلايا العملاقة. المراجعة الدقيقة لشكل الخلية هي المفتاح لتحديدها - بينما تُظهر الخلايا العملاقة باينًا كبيرًا في توزيعات حجم الخلايا وأشكالها في الأورام، تحتوي سرطانات المشيمة باستمرار على الخلايا الغاذية المتزامنة والخلايا الغاذية الخلوية فقط.[19] يمكن أيضًا التمييز بين سرطان الخلايا العملاقة وسرطان المشيمة الرئوي الأولي على أساس السمات البنائية الدقيقة بواسطة المجهر الإلكتروني، على الرغم من أن المجهر الإلكتروني غير قابل للتطبيق على نطاق واسع حتى الآن.[20] في بعض الأحيان، قد يُخطئ البعض في تشخيص ورم الخلايا العملاقة العظمية الناتج عن ورم الخلايا العملاقة العظمي الأولي - حيث يمكن أن يتصرف هذا الأخير كورم حميد، أو خبيث بشكل صريح،[21][22] أو على حافة في سلوكه السريري.[23][24]
مواقع النقائل
تُعد أورام الخلايا العملاقة العظمية ملحوظة بشكل خاص بين سرطانات الرئة لميلها غير المعتاد للغاية إلى الانتشار إلى الأمعاء الدقيقة، مما يتسبب أحيانًا في انسداد ونزيف حاد و/أو انغلاف. ولوحظت هذه الخاصية السريرية لأورام الخلايا العملاقة في حالات امتدت لأكثر من نصف قرن.[25][26] يبدو أن الصائم هو الموقع المفضل لانتشار أورام الخلايا العملاقة داخل الأمعاء الدقيقة. ينتشر سرطان الخلايا العملاقة أيضًا في كثير من الأحيان إلى العظام،[21] والغدة الكظرية، والدماغ،[17] والرئة، والكبد، والكلى. ومن المرجح بشكل خاص أن تسبب نقائل الدماغ من سرطان الخلايا العملاقة نزيفًا دماغيًا كبيرًا مقارنة بمتغيرات سرطان الرئة الأخرى، وربما يرجع ذلك إلى زيادة كبيرة في معدلات تكاثر الخلايا البطانية وتكوين الأوعية الدموية الجديدة، ونمو أنسجة الورم، والنخر الواسع النطاق، والطبيعة التسللية المحلية العدوانية لخلايا سرطان الخلايا العملاقة.[17]
التسبب في المرض
أظهرت العديد من الدراسات، سواءً في عينات أورام الخلايا العملاقة أو في سلالات الخلايا، إعادة ترتيب وتضخيم جين الورم c-myc، أحيانًا بالتزامن مع طفرات في جين K-ras.[27][28] وقد تبين أن الإفراط في التعبير عن عامل نمو بطانة الأوعية الدموية (VEGF) يحدث في سرطان الخلايا العملاقة، ويُعتقد أنه مرتبط بإمكانية انتشاره العالية.[13] توجد خلايا عملاقة خبيثة مماثلة لتلك الموجودة في سرطان الخلايا العملاقة بشكل شائع في حالات سرطان الرئة المصحوبة بنمط سرطان خلايا صافية رئيسي أو ثانوي بارز. وقد افترض أنها مشتقة من خلية جذعية خبيثة متعددة القدرات غير متمايزة يتم إنشاؤها في القصيبات البعيدة عبر مسار أورم جيني غير معروف حتى الآن أو محرك أورم جيني.[12] ومن الناحية البنيوية الفائقة، غالبًا ما تحتوي الخلايا العملاقة الخبيثة على تراكمات من الخيوط الدقيقة مرتبة في دوامات بالقرب من نواة الخلية. تبدو هذه الكيانات متشابهة في بنيتها مع الخيوط الدقيقة والحزم الموجودة في الخلية D1 في الجهاز الصماء المعوي البنكرياسي، وقد اقترح أن خلايا D1 هذه قد تكون الخلية الجذعية السرطانية لبعض الخلايا العملاقة على الأقل. كما تم إنتاج هياكل خيوط حلزونية متطابقة المظهر في بعض خلايا مجرى الهواء لدى الحيوانات بعد العلاج بالنيتروزامينات المسرطنة.[29] وقد اقترحت الدراسات البنيوية الفائقة أن الخلايا العملاقة الخبيثة في الخلايا العملاقة هي من سلالة الأديم الباطن.[30] أورام سريعة النمو بشكل ملحوظ.[17]
أورام مركبة/متعددة المراحل تحتوي على خلايا عملاقة
توجد الخلايا العملاقة الخبيثة بشكل شائع - وتختلف نسبتها النسبية بدرجات متفاوتة - في كل من الأورام الأولية والنقائل للعديد من أنواع سرطان الرئة المختلفة. وقد لاحظ عدد من الباحثين أن الخلايا العملاقة الخبيثة الغريبة تحدث بشكل أكثر شيوعًا في الأورام الأولية والثانوية - بما في ذلك أي "رواسب" متبقية من الورم - التي عولجت سابقًا بالعلاج الكيميائي و/أو العلاج الإشعاعي في بروتوكولات مساعدة أو علاجات جديدة مساعدة.[30]
خصائص الأشعة
غالبًا ما يظهر سرطان الخلايا العملاقة الخبيثة على شكل كتلة محيطية كبيرة ذات تجويف شديد.[31] في دراسة شعاعية أجريت على ما يقرب من 2000 مريض بسرطان الرئة ونُشرت قبل 50 عامًا، تبين أن 3.4% من سرطانات الرئة عبارة عن كتل مجوفة،[32] وكان معظمها سرطان الخلايا الحرشفية. في عدد من حالات التجويف الشديد، تتكون بقايا الورم المستأصلة من حافة رقيقة فقط من الخلايا المتكاثرة.
التصوير المقطعي بالإصدار البوزيتروني
في مسح التصوير المقطعي بالإصدار البوزيتروني (PET)، وُجد أن سرطان الخلايا العملاقة يتمتع بقيم امتصاص موحدة عالية جدًا للجلوكوز المشع، وهي قيم أعلى بكثير إحصائيًا من المتغيرات النسيجية الأخرى لسرطان الرئة.[33]
المسارات الأيضية
يشير التصوير المقطعي بالإصدار البوزيتروني (PET) إلى أن أورام الخلايا العملاقة هي أورام ذات أيض سريع بشكل خاص، وأن المسارات الأيضية لأورام الخلايا العملاقة قد تعتمد بشكل غير عادي على تحلل الجلوكوز أو ترتبط به.[33]
متلازمات نظير الورم
عُرفت أورام الخلايا العملاقة منذ فترة طويلة بإفرازها لوحدة بيتا الفرعية من موجهة الغدد التناسلية المشيمية البشرية (بيتا-HCG)،[34] غالبًا بكميات كبيرة، مما قد يؤدي إلى مستويات عالية جدًا من هرمون الإستروجين وتضخم الثدي المؤلم لدى الذكور كعلامات نظير الورم.[35] تشتهر سرطانات الرئة ذات الخلايا العملاقة بإنتاجها وإفرازها لعامل تحفيز مستعمرات الحبيبات (G-CSF).[28][36] كما أُفيد بأن أورام الخلايا العملاقة تنتج منشط البلازمينوجين كظاهرة نظيرة للورم.[9]
العلاج
نظرًا لندرته، لم تُجرَ أي تجارب سريرية عشوائية لعلاج سرطان الخلايا العملاقة، وجميع المعلومات المتاحة مستمدة من سلاسل مؤسسية صغيرة بأثر رجعي أو بيانات وصفية متعددة المراكز.[37]
التشخيص
لطالما اعتُبرت سرطانات الرئة ذات الخلايا العملاقة أورامًا خبيثة شديدة العدوانية، تنمو بسرعة كبيرة، ولها تشخيص سيء للغاية.[38][14][39][28][40] أشارت العديد من الدراسات الصغيرة إلى أن تشخيص أورام الرئة ذات الخلايا العملاقة أسوأ من تشخيص معظم أشكال سرطان الرئة غير صغير الخلايا (NSCLC) الأخرى،[11] بما في ذلك سرطان الخلايا الحرشفية،[40] وسرطان الخلايا المغزلية.[40] يختلف معدل البقاء على قيد الحياة لمدة خمس سنوات في سرطان الخلايا العملاقة بين الدراسات، ولكنه يُعتبر منخفضًا جدًا بشكل عام. وقد أفاد معهد علم الأمراض التابع للقوات المسلحة الأمريكية بنسبة 10%،[41] وفي دراسة فحصت أكثر من 150,000 حالة سرطان رئة، تم إعطاء نسبة 11.8%.[5] ومع ذلك، في التقرير الأخير، استند رقم 11.8% إلى بيانات شملت سرطان الخلايا المغزلية، وهو نوع يُعتبر عمومًا أقل سوءًا من سرطان الخلايا المغزلية الكبير.[11] لذلك، فإن احتمالية بقاء سرطان الخلايا المغزلية الكبير "الخالص" على قيد الحياة ربما تكون أقل من الرقم المذكور. في مراجعة قاعدة البيانات الكبيرة لعام 1995 التي أجراها ترافيس وزملاؤه، كان سرطان الخلايا العملاقة ثالث أسوأ تشخيص بين 18 شكلًا نسيجيًا من سرطان الرئة. (كان متوسط بقاء سرطان الخلايا الصغيرة وسرطان الخلايا الكبيرة أقصر فقط).[5] لقد نمت معظم سرطانات الخلايا المغزلية الكبير بالفعل وغزت محليًا و/أو إقليميًا، و/أو انتشرت بالفعل بعيدًا، وهي غير قابلة للعلاج الجراحي، وقت التشخيص.[14]
علم الأوبئة
إن المعدل الحقيقي للإصابة بسرطان الخلايا العملاقة للرئة وانتشاره ومعدل الوفيات به غير معروف عمومًا نظرًا لنقص بيانات السرطان الدقيقة على المستوى الوطني. يُعرف أن هذا النوع من الأورام نادر جدا في جميع الفئات السكانية التي خضعت للفحص. في دراسة أمريكية لقاعدة بيانات لأكثر من 60,000 حالة سرطان رئة، كون سرطان الخلايا العملاقة للرئة بين 0.3% و0.4% من الأورام الخبيثة الرئوية الأولية، مع معدل إصابة معدل حسب العمر يبلغ حوالي 3 حالات جديدة لكل مليون شخص سنويًا. مع تشخيص ما يقرب من 220,000 حالة سرطان رئة في الولايات المتحدة سنويًا،[42] تشير النسبة إلى تشخيص ما يقرب من 660 و880 حالة جديدة لدى الأمريكيين سنويًا.[5][43] مع ذلك، في سلسلة أحدث من 4212 حالة سرطان رئة متتالية، تم تحديد آفة واحدة فقط (0.024%) على أنها سرطان خلايا عملاقة "خالص" بعد التقطيع الكامل لجميع أنسجة الورم المتاحة.[33] في حين تشير بعض الأدلة إلى أن سرطان الخلايا العملاقة "الخالص" ربما كان أكثر شيوعًا منذ عدة عقود، حيث حددت إحدى السلاسل 3.4% من جميع سرطانات الرئة على أنها أورام خبيثة ذات خلايا عملاقة،[44] يمكن أن يكون هذا انعكاس الرقم تظهر معظم سلاسل الحالات والتقارير المنشورة عن سرطانات الرئة التي تحتوي على خلايا عملاقة أنها يتم تشخيصها بشكل متكرر أكثر لدى الرجال منها لدى النساء،[15][40] مع إظهار بعض الدراسات نسبًا عالية للغاية بين الذكور والإناث (12:1 أو أكثر). في دراسة أجريت على أكثر من 150,000 شخص مصاب بسرطان الرئة في الولايات المتحدة، كانت نسبة الجنس أعلى بقليل من 2:1، حيث كانت نسبة الإصابة بسرطان الخلايا العملاقة لدى النساء أعلى نسبيًا (0.4%) من الرجال (0.3%).[5] وقد تم الإبلاغ عن تشخيص سرطان الخلايا العملاقة في فئة عمرية أصغر بكثير من جميع سرطانات الخلايا غير الصغيرة التي تُعتبر مجموعة.[15][38] ومع ذلك، مثل جميع سرطانات الرئة تقريبًا، فإن سرطان الخلايا العملاقة نادر للغاية لدى الشباب جدًا: في برنامج SEER الأمريكي، تم تسجيل حالتين فقط حدثتا لدى أشخاص تقل أعمارهم عن 30 عامًا بين عامي 1983 و1987.[5] وقد قُدِّر متوسط العمر عند تشخيص هذه الأورام بـ 60 عامًا.[15] الغالبية العظمى من الأفراد المصابين بسرطان الخلايا العملاقة هم من المدخنين الشرهين.[15] على الرغم من أن تعريفات "المركزي" و"المحيطي" يمكن أن تختلف بين الدراسات،[15] إلا أن سرطان الخلايا القاعدية الخليجية يُشخص باستمرار بشكل أكثر تكرارًا في محيط الرئة.[15] في مراجعة للأدبيات التي جمعها كالينبرغ وزملاؤه، نشأ أقل من 30% من سرطان الخلايا العملاقة في السرة أو أجزاء أخرى من الشجرة الرئوية "المركزية".[38] كما افترض وجود ميل كبير لنشأة سرطان الخلايا العملاقة في الرئة في الفصوص العلوية من المرضى.[15]
التاريخ
تنسب معظم المصادر إلى ناش وستاوت نشر أول تقرير مفصل في الأدبيات الطبية يعترف بسرطان الخلايا العملاقة بأنه مرض إكلينيكي متميز في عام 1958.[45] ومع ذلك، هناك بعض الأدلة التي تشير إلى أن هذا النمط الظاهري للورم قد وُصف في وقت مبكر من عام 1951.[46] في تقرير عن 3 حالات من سرطان الرئة ذو الخلايا العملاقة نُشر عام 1961 بواسطة Z.M. Naib، يستشهد المؤلف بدراستين سابقتين متعلقتين بسرطان الرئة ذو الخلايا العملاقة - إحداهما نُشرت عام 1951 بواسطة M.M. Patton وزملائه،[47] والأخرى نُشرت عام 1955 بواسطة Walton and Pryce.[48] في عام 1969، نسب الدكتور ألكسندر كينيدي، في سلسلة حالات من 3 حالات سرطان الرئة ذو الخلايا العملاقة نُشرت عام 1969،[14] إلى هادلي وبولوك أول استخدام لمصطلح "سرطان الخلايا العملاقة" قبل 16 عامًا.[49] تم تأكيد سرطان الرئة ذو الخلايا العملاقة لأول مرة على أنه ورم ظهاري (وليس ساركوما متعدد الأشكال غير متمايز) في عام 1961.[50] في عامي 1964 و1965، طرحت نظريات افتراض أن سرطانات الخلايا العملاقة هي سرطانات غدية غير متمايزة،[51] وفي بعض الحالات، كان يُعتقد أنها مشتقة من سرطانات غدية ذات خلايا صافية.[52]
المراجع
- ^ ا ب ج د ه و ز ح ط ي يا يب "Wayback Machine" (PDF). web.archive.org. اطلع عليه بتاريخ 2025-04-16.
- ^ Roggli VL، Vollmer RT، Greenberg SD، McGavran MH، Spjut HJ، Yesner R (1985). "Lung cancer heterogeneity: a blinded and randomized study of 100 consecutive cases". Hum Pathol. ج. 16 ع. 6: 569–79. DOI:10.1016/s0046-8177(85)80106-4. PMID:2987102.
- ^ Rossi G، Marchioni A، Sartori G، Longo L، Piccinini S، Cavazza A (2007). "Histotype in non-small-cell lung cancer therapy and staging: The emerging role of an old and underrated factor". Curr Respir Med Rev. ج. 3: 69–77. DOI:10.2174/157339807779941820. S2CID:52904357.
- ^ Vincent MD (2009). "Optimizing the management of advanced non-small-cell lung cancer: a personal view". Curr Oncol. ج. 16 ع. 4: 9–21. DOI:10.3747/co.v16i4.465. PMC:2722061. PMID:19672420.
- ^ ا ب ج د ه و Travis WD، Travis LB، DeVesa SS (1995). "Lung Cancer". Cancer. ج. 75 ع. 1 Suppl: 191–202. DOI:10.1002/1097-0142(19950101)75:1+<191::AID-CNCR2820751307>3.0.CO;2-Y. PMID:8000996. S2CID:34718856.
- ^ World Health Organization (1981). Histological typing of Lung Tumours (ط. 2nd). Geneva: World Health Organization.
- ^ Brambilla E، Travis WD، Colby TV، Corrin B، Shimosato Y (ديسمبر 2001). "The new World Health Organization classification of lung tumours". Eur. Respir. J. ج. 18 ع. 6: 1059–68. DOI:10.1183/09031936.01.00275301. PMID:11829087. S2CID:3108488.
- ^ ا ب Hiroshima K، Dosaka-Akita H، Usuda K، وآخرون (2011). "Cytological characteristics of pulmonary pleomorphic and giant-cell carcinomas". Acta Cytol. ج. 55 ع. 2: 173–9. DOI:10.1159/000320860. PMID:21325803. S2CID:39144324.
- ^ ا ب ج د ه و Davidson JF، McNicol GP، Frank GL، Anderson TJ، Douglas AS (يناير 1969). "Plasminogen-activator-producing tumour". Br Med J. ج. 1 ع. 5636: 88–91. DOI:10.1136/bmj.1.5636.88. PMC:1982019. PMID:5761832.
- ^ Cacić M، Oberman B، Dvornik G (ديسمبر 1989). "Investigation of the applicability of histological classification of bronchial carcinoma according to the World Health Organization". Tumori. ج. 75 ع. 6: 580–2. DOI:10.1177/030089168907500613. PMID:2482566. S2CID:11142517.
- ^ ا ب ج د ه Matsui K، Kitagawa M (مايو 1991). "Spindle cell carcinoma of the lung. A clinicopathologic study of three cases". Cancer. ج. 67 ع. 9: 2361–7. DOI:10.1002/1097-0142(19910501)67:9<2361::aid-cncr2820670925>3.0.co;2-3. PMID:1707339.
- ^ ا ب ج Wang NS، Seemayer TA، Ahmed MN، Knaack J (يناير 1976). "Giant cell carcinoma of the lung. A light and electron microscopic study". Hum. Pathol. ج. 7 ع. 1: 3–16. DOI:10.1016/s0046-8177(76)80003-2. PMID:172430.
- ^ ا ب Jiang DF، Lu YL، Qiu ZY، وآخرون (2003). "Study of differential expression of molecules affecting the metastatic potential between highly and poorly metastatic human lung giant cell carcinoma". Zhonghua Zhong Liu Za Zhi. ج. 25: 131–4.
- ^ ا ب ج د ه و Kennedy A (مايو 1969). "Pathology and survival in operable cases of giant-cell carcinoma of the lung". J. Clin. Pathol. ج. 22 ع. 3: 354–60. DOI:10.1136/jcp.22.3.354. PMC:474089. PMID:5784984.
- ^ ا ب ج د ه و ز ح ط ي Kim TH، Kim SJ، Ryu YH، وآخرون (أغسطس 2004). "Pleomorphic carcinoma of lung: comparison of CT features and pathologic findings". Radiology. ج. 232 ع. 2: 554–9. DOI:10.1148/radiol.2322031201. PMID:15215543.
- ^ Shirakusa T، Shigematsu N، Koga T، Yamagata Y (1980). "Giant cell carcinoma arising in a pulmonary bulla". Scand J Thorac Cardiovasc Surg. ج. 14 ع. 3: 307–9. DOI:10.3109/14017438009101017. PMID:7221506.
- ^ ا ب ج د Hagihara N، Abe T، Wakamiya T، Sugita Y، Watanabe M، Tabuchi K (2010). "A case of brain metastasis from pulmonary giant cell carcinoma". Kurume Med J. ج. 57 ع. 1–2: 39–41. DOI:10.2739/kurumemedj.57.39. PMID:21727764.
- ^ Spivach A, Borea B, Bertoli G, Daris G (Jul 1976). "[Primary lung neoplasm of rare incidence: giant cell carcinoma]". Minerva Med. (بالإيطالية). 67 (34): 2233–49. PMID:986035.
- ^ Travis WD (نوفمبر 2010). "Sarcomatoid neoplasms of the lung and pleura". Arch. Pathol. Lab. Med. ج. 134 ع. 11: 1645–58. DOI:10.5858/2010-0086-RAR.1. PMID:21043818.
- ^ Hayakawa K، Takahashi M، Sasaki K، Kawaoi A، Okano T (يناير 1977). "Primary choriocarcinoma of the lung: case report of two male subjects". Acta Pathol. Jpn. ج. 27 ع. 1: 123–35. PMID:557868.
- ^ ا ب Willebrand H, Wernitsch W, Elmohamed A (Sep 1970). "[Pulmonary metastases of a giant-cell carcinoma in the bone—benign or malignant?]". Chirurg (بالألمانية). 41 (9): 419–23. PMID:5471024.
- ^ Huang L، Xu J، Wood DJ، Zheng MH (مارس 2000). "Gene expression of osteoprotegerin ligand, osteoprotegerin, and receptor activator of NF-kappaB in giant cell tumor of bone: possible involvement in tumor cell-induced osteoclast-like cell formation". Am. J. Pathol. ج. 156 ع. 3: 761–7. DOI:10.1016/s0002-9440(10)64942-5. PMC:1876848. PMID:10702390.
- ^ Werner M (ديسمبر 2006). "Giant cell tumour of bone: morphological, biological and histogenetical aspects". Int Orthop. ج. 30 ع. 6: 484–9. DOI:10.1007/s00264-006-0215-7. PMC:3172738. PMID:17013643.
- ^ Pai SB، Lalitha RM، Prasad K، Rao SG، Harish K (سبتمبر 2005). "Giant cell tumor of the temporal bone—a case report". BMC Ear Nose Throat Disord. ج. 5: 8. DOI:10.1186/1472-6815-5-8. PMC:1253509. PMID:16162299.
- ^ Thomas C (1962). "[Giant cell carcinoma of the lungs]". Frankf Z Pathol (بالألمانية). 72: 302–8. PMID:13981042.
- ^ Wellmann KF، Chafiian Y، Edelman E (فبراير 1969). "Small bowel perforation from solitary metastasis of clinically undetected pulmonary giant cell carcinoma". Am. J. Gastroenterol. ج. 51 ع. 2: 145–50. PMID:5776147.
- ^ Le Doussal JM، Gruaz-Guyon A، Martin M، Gautherot E، Delaage M، Barbet J (يونيو 1990). "Targeting of indium 111-labeled bivalent hapten to human melanoma mediated by bispecific monoclonal antibody conjugates: imaging of tumors hosted in nude mice". Cancer Res. ج. 50 ع. 11: 3445–52. PMID:2334941. مؤرشف من الأصل في 2025-01-23.
- ^ ا ب ج Taya Y، Hosogai K، Hirohashi S، وآخرون (ديسمبر 1984). "A novel combination of K-ras and myc amplification accompanied by point mutational activation of K-ras in a human lung cancer". EMBO J. ج. 3 ع. 12: 2943–6. DOI:10.1002/j.1460-2075.1984.tb02236.x. PMC:557793. PMID:6098458.
- ^ Carstens PH، Broghamer WL (أبريل 1978). "Duodenal carcinoid with cytoplasmic whorls of microfilaments". J. Pathol. ج. 124 ع. 4: 235–8. DOI:10.1002/path.1711240408. PMID:569192. S2CID:43844600.
- ^ ا ب Sidhu GS (يوليو 1979). "The endodermal origin of digestive and respiratory tract APUD cells. Histopathologic evidence and a review of the literature". Am. J. Pathol. ج. 96 ع. 1: 5–20. PMC:2042351. PMID:37740.
- ^ Culiner MM، Abouav J، Reich SB (نوفمبر 1958). "Cavitary carcinoma of the lung". Calif Med. ج. 89 ع. 5: 355–8. PMC:1512515. PMID:13585165.
- ^ Strang C، Simpson JA (مارس 1953). "Carcinomatous abscess of the lung". Thorax. ج. 8 ع. 1: 11–26. DOI:10.1136/thx.8.1.11. PMC:1019223. PMID:13038734.
- ^ ا ب ج Park JS، Lee Y، Han J، وآخرون (2011). "Clinicopathologic outcomes of curative resection for sarcomatoid carcinoma of the lung". Oncology. ج. 81 ع. 3–4: 206–13. DOI:10.1159/000333095. PMID:22076573. S2CID:25558721.
- ^ Dailey JE، Marcuse PM (أغسطس 1969). "Gonadotropin secreting giant cell carcinoma of the lung". Cancer. ج. 24 ع. 2: 388–96. DOI:10.1002/1097-0142(196908)24:2<388::aid-cncr2820240222>3.0.co;2-7. PMID:5796783. S2CID:3506191.
- ^ Yaturu S، Harrara E، Nopajaroonsri C، Singal R، Gill S (2003). "Gynecomastia attributable to a human chorionic gonadotropin-secreting giant cell carcinoma of the lung". Endocr Pract. ج. 9 ع. 3: 231–5. DOI:10.4158/EP.9.3.233. PMID:12917067.
- ^ Kameda T؛ Kodama T؛ Shimosato Y (1982). Shimosato Y؛ Melamed MR؛ Nettesheim P (المحررون). Morphogenesis of Lung Cancer. Boca Raton, Florida: CRC Press. ج. 2. ص. 107–29.
- ^ Bae HM، Min HS، Lee SH، Kim DW، Chung DH، Lee JS، Kim YW، Heo DS (أكتوبر 2007). "Palliative chemotherapy for pulmonary pleomorphic carcinoma". Lung Cancer. ج. 58 ع. 1: 112–5. DOI:10.1016/j.lungcan.2007.05.006. PMID:17574296.
- ^ ا ب ج Kallenberg F، Jaqué J (1979). "Giant cell carcinoma of the lung. Clinical and pathological assessment. Comparison with other large-cell anaplastic bronchogenic carcinomas". Scand J Thorac Cardiovasc Surg. ج. 13 ع. 3: 343–6. DOI:10.3109/14017437909100576. PMID:542838.
- ^ Razzuk MA، Urschel HC، Albers JE، Martin JA، Paulson DL (يونيو 1976). "Pulmonary giant cell carcinoma". Ann. Thorac. Surg. ج. 21 ع. 6: 540–5. DOI:10.1016/s0003-4975(10)63926-4. PMID:1275605.
- ^ ا ب ج د Zhao ZL, Song N, Huang QY, Liu YP, Zhao HR (Feb 2007). "[Clinicopathologic features of lung pleomorphic (spindle/giant cell) carcinoma—a report of 17 cases]" [Clinicopathologic features of lung pleomorphic (spindle/giant cell) carcinoma—a report of 17 cases]. AI Zheng (بالصينية). 26 (2): 183–8. PMID:17298750. (Chinese text) نسخة محفوظة 2013-01-15 at Archive.is
- ^ Colby TV، Koss MN، Travis WD (1995). "Tumors of the lower respiratory tract". Atlas of Tumor Pathology. Washington DC: Armed Forces Institute of Pathology. ص. 259–75.
- ^ "Fact Sheet: Cancer of the Lung and Bronchus". National Cancer Institute, SEER Program. مؤرشف من الأصل في 2025-04-11. اطلع عليه بتاريخ 2012-02-24.
- ^ Martin LW، Correa AM، Ordonez NG، وآخرون (سبتمبر 2007). "Sarcomatoid carcinoma of the lung: a predictor of poor prognosis". Ann. Thorac. Surg. ج. 84 ع. 3: 973–80. DOI:10.1016/j.athoracsur.2007.03.099. PMID:17720411.
- ^ Hellstrom HR، Fisher ER (1963). "Giant cell carcinoma of lung". Cancer. ج. 16 ع. 8: 1080–8. DOI:10.1002/1097-0142(196308)16:8<1080::aid-cncr2820160816>3.0.co;2-v. PMID:14050012.
- ^ Nash AD، Stout AP (1958). "Giant cell carcinoma of the lung; report of 5 cases". Cancer. ج. 11 ع. 2: 369–76. DOI:10.1002/1097-0142(195803/04)11:2<369::aid-cncr2820110222>3.0.co;2-8. PMID:13511359. S2CID:40340336.
- ^ Naib ZM (1961). "Giant cell carcinoma of the lung: cytological study of the exfoliated cells in sputa and bronchial washings". Dis Chest. ج. 40: 69–73. DOI:10.1378/chest.40.1.69. PMID:13727525. S2CID:19208368.
- ^ Patton MM، McDonald JR، Moersch HJ (1951). "Bronchogenic large cell carcinoma". J Thorac Cardiovasc Surg. ج. 22 ع. 1: 88–93. PMID:14851490.
- ^ Walter JB، Pryce DM (يونيو 1955). "The histology of lung cancer". Thorax. ج. 10 ع. 2: 107–16. DOI:10.1136/thx.10.2.107. PMC:1019475. PMID:14396845.
- ^ Hadley GG، Bullock WK (ديسمبر 1953). "Autopsy reports of pulmonary carcinoma; survey in Los Angeles County Hospital for 1951". Calif Med. ج. 79 ع. 6: 431–3. PMC:1521859. PMID:13106728.
- ^ Ozzello L، Stout AP (1961). "The epithelial origin of giant cell carcinoma of the lung confirmed by tissue culture. Report of a case". Cancer. ج. 14 ع. 5: 1052–6. DOI:10.1002/1097-0142(196109/10)14:5<1052::aid-cncr2820140521>3.0.co;2-d. PMID:13731858. S2CID:6846264.
- ^ Friedberg EC (فبراير 1965). "Giant-Cell Carcinoma of the Lung: A dedifferentiated Adenocarcinoma". Cancer. ج. 18 ع. 2: 259–64. DOI:10.1002/1097-0142(196502)18:2<259::aid-cncr2820180219>3.0.co;2-f. PMID:14254083. S2CID:12195106.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعMorganMacKenzie








